A termodinâmica (do grego therme = calor e dynamis = movimento) é a parte da física que estuda as relações entre calor, temperatura, trabalho e energia. Abrange o comportamento geral dos sistemas físicos em condições de equilíbrio ou próximas dele.
TRABALHO TERMODINÂMICO (τ)
Construímos uma máquina térmica com uma finalidade específica: a realização de trabalho.
Em física, trabalho significa aplicação de uma força com um consequente deslocamento do objeto em questão.
No caso da máquina térmica, existe uma transformação de energia térmica em movimento, ou seja transformação de energia térmica em trabalho.
Um exemplo de processo termodinâmico onde ocorre a realização de trabalho é o funcionamento de um motor de combustão interna (motor de carro). Depois da mistura de combustível e comburente (gasolina e ar atmosférico, por exemplo), dentro do cilindro, essa mistura recebe uma fagulha das velas do motor, se expande devido ao aquecimento da explosão fazendo com que o cilindro seja violentamente movimentado no sentido da expansão dos gases. Ao movimentar-se, o pistão inicia uma complexa cadeia de eventos que culmina na movimentação das rodas do carro, realizando assim sua função de movimento, ou seja, de realização de trabalho.
* Pressão constante
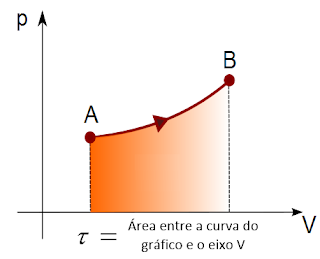
Graficamente:
Unidade do trabalho:
Trabalho sob pressão constante:
- V aumenta (V2 > V1) => sistema realiza trabalho => τ > 0
- V diminui (V2 < V1) =>sistema recebe trabalho => τ < 0
- V constante (V2 = V1) =>sistema não troca trabalho => τ = 0
ENERGIA INTERNA DE UM GÁS (U)
A energia interna de um gás perfeito é a soma das energias cinéticas médias de todas as suas moléculas. A energia interna de um gás perfeito está diretamente associada à sua temperatura. Quando um sistema (gás) recebe uma determinada quantidade de calor (Q), sofre um aumento de sua energia interna(ΔU) e, consequentemente um aumento de temperatura (ΔT). Assim, a variação de energia interna para os gases monoatômicos é dada por:
- Se Δt> 0 => ΔU > 0 : energia interna aumenta.
- Se Δt< 0 => ΔU < 0 : energia interna diminui.
- Se Δt= 0 => ΔU = 0 : energia interna não varia
Lei de Joule: a energia interna de uma dada massa de gás ideal é
função exclusiva da temperatura, não dependendo do processo.
PRIMEIRA LEI DA TERMODINÂMICA
O Primeiro Princípio da Termodinâmica estabelece uma equivalência entre o trabalho termodinâmico e o calor, trocados entre um sistema e o seu exterior. Ele é um princípio de conservação de energia.











Nenhum comentário:
Postar um comentário